-
 مدیر بازنشسته
مدیر بازنشسته
-
 مدیر بازنشسته
مدیر بازنشسته

تاریخچه کار
بشر از زمانی که خود راشناخت در پی کار و فعالیت بوده ودر هر زمان دستخوش تحولاتی گردیده است . وجود ابزار کار شاید قدیمی ترین تحولی باشد که در زندگی بشر بوجود آمده است . زمانی ابزار سنگی و بعدا با پیدایش آهن و فلزات ابزار فلزی جایگزین آن شد و تا موقعی که آن ابزار جز به نیروی عضلانی انسان حرکت نمی کردند ابزار دستی اساسی ترین عنصر تولید بوده است لیکن با ابداع کشاورزی ودامداری . آغاز شهرنشینی و گسترش شهرها ورود ماشین آلات . توسعه آن و تجلی عصر ماشین . انقلابی بس عظیم در کسترش فعالیتهای انسانی پدیدار شد . در بررسی تاریخچه کار از عصر ابزار دستی تا عصر ماشین به دوره های دیگری نیز برمی خوریم که در زندگی و کار انسانها سایه افکنده است از این رو تاریخچه کار را بطور کلی می توان در دوره هایی مشتمل بر عصر ابزار دستی . دوره بردگی . کار زراعتی . کار زنان و عصر ماشین مورد بررسی و مطالعه قرار داد .
تاریخچه بهداشت شغلی ( حرفه ای )
تا قرن شانزدهم میلادی در کتب طبی به بهداشت شغلی و ارتباط بیماریهای مختلف با شغل افراد اشاره قابل توجهی نشده است . از قرن شانزدهم به بعد در تاریخ به چهره های درخشانی بر می خوریم که تمام عمر خود را صرف تشخیص وجلوگیری از بیماریهای ناشی از کار نموده و خدمات با ارزشی انجام داده اند .
اولین فردی که آثار ارزنده ای در موردد بهداشت شغلی از خود به یادگار گذاشته است طبیبی از ناحیه ساکسونی در ایتالیا بنام اگریکولما بود او کتابی در 12 جلد درباره اکتشافات و استخراج فلزات . ابزار کار . حوادث و بیماریهای ناشی از کار و ... نوشت که در سال 1556 منتشر شد . بعداز اودر سال 1567 پزشک دیگری اهل سوئیس بنام پاراسلسوس کتابی درباره بیماری های وابسته به شغل در بین کارکنان معدن ذوب و فلزات منتشر کرد . در سال 1633 پدر طب کار یا همان رامازینی بدنیا آمد که یکی از پیشقدمان بزرگ قرن 17 در زمینه بهداشت کار می باشد . کتاب معروفش در باره بیماریهای حرفه ای در سال 1700 میلادی منتشر شد . او برای اولین بار به پزشکان توصیه کرد که علاوه بر سوالات که در زمان معاینه از بیماران می پرسیدند از همه بپرسند شغل شما چیست این جمله کوتاه نقطه عطفی در تاریخ طب کار بشمار آمده است .
پس از آن می توان به وضع قانون کار در سال 1832 در انگلستان اشاره کرد در میان پزشکان قرن نوزدهمی که در این رشته فعالیت داشته میتوان از دو پزشک انگلیسی به نامهای چارلز تاکرا و سرتوماس لک نام برد .
تعریف بهداشت حرفه ای
تعریف کلاسیک : علمی که شناسائی . اندازه گیری و مقایسه با استاندارد و کنترل عوامل زیان آور محیط کار شامل عوامل شیمیائی فیزیکی بیولوزیکی مکانیکی و روانی که روی سلامتی کارگران یا شاغلین اثر می گذارد رابه عهده دارد
هدف بهداشت حرفه ای
اهداف کلی بهداشت حرفه ای را می توان بدین ترتیب نام برد :
1- ارتقاء سطح سلامت جسمی وروانی و اجتماعی شاغلی
2- پیشگیری از بروز بیماریهای حرفه ای
3- جلوگیری از بروز حوادث ناشی از کار
4- انتخاب کارگر مناسب که از لحاظ جسمی و روانی متناسب با کار باشد
عوامل زیان آور محیط کار بطور کلی به چهار گروه تقسیم می شوند
1- عوامل فیزیکی زیان آور محیط کار
این عوامل خود به 5 دسته تقسیم می شوند
* صدا
هر چیزی که شنیده میشود صدا نام دارد . امروزه صدا جزئی از زندگی انسان رادر بر می گیرد وبه عنوان یکی از خطرات شغلی و صنعتی به شمار می آید . صدا باعث افزایش ضربان قلب . افزایش فشار خون . سردرد سرگیجه واستفراغ ودر نهایت باعث کری شغلی می شود . حد استاندارد صدا در محیط کار 85 دسی بل در 8 ساعت کاری است .
برای پیشگیری از عوارض صدا به نکات ذیل باید توجه کرد
- معاینات قبل از استخدام و دوره ای
- استفاده از وسایل حفاظت فردی
- کاهش صدا در دستگاه
جوشکاریها . تراشکاری ها .نجاریها . چوب بری ها سنگ بری ها و ... در معرض عوارض ناشی از صدا هستند .
* ارتعاش
حرکت نوسانی اجسام است که از ماشین ها و تجهیزات تولید و اثرات آن ناشی از تماس با آن است . ارتعاش در موارد خفیف باعث سردرد وناراحتی عمومی ودر موارد شدید باعث سرئرئ . سرگیجه و استفراغ می شود . ارتعاش در دست باعث رنگ پریدگی در انگشت . درد .خارش و مورمور شدن دست می شود . ارتعاش بیشتر در دست وبازو و یا تمام بدن ( رانندگان ) منتقل میشود و عوارض ایجاد می کند
برای کنترل و پیشگیری از عوارض ارتعاش می توان اقدامات ذیل را انجام داد
- میراکردن ارتعاش به دست و بازو ( هدایت ابزار از فاصله دور . میرا کردن ابزار از درون ویا بدنه ابزار )
- کاهش زمان کار با دستگاه تولید ارتعاش
- در رانندگان استفاده از سیستم فنر بندی صندلی راننده و نیز قرار دادن بالشی نرم میان راننده و صندلی
* روشنائی
امروزه روشنائی برای کارگاهها اهمیتی ویزه یافته است زیرا کمبود روشنائی در محیط کار . افزون بر ایجاد خستگی اعصاب . آسیب های دیگر به سلامت و بینائی کارگر وارد می آورد
روشنائی در کارگاه به دو صورت تامین می گردد
- روشنائی طبیعی ( نور خورشید )
می توان با تعبیه پنجره مناسب این روشنائی را ایجاد کرد که نسبت به روشنائی مصنوعی برتر ی دارد
- روشنائی مصنوعی
در روشنائی مصنوعی از لامپ های الکتریکی استفاده می گردد که باید در طراحی آن دقت شود تا باعث خیرگی نشود
قالی بافان . طراحان و اپراتورها و ... در معرض عوارض ناشی از روشنائی هستند
* اشعه
گونه ای از انرزی است که در خلاء یا ماده منتشر می شود
- یونساز - غیر یونساز
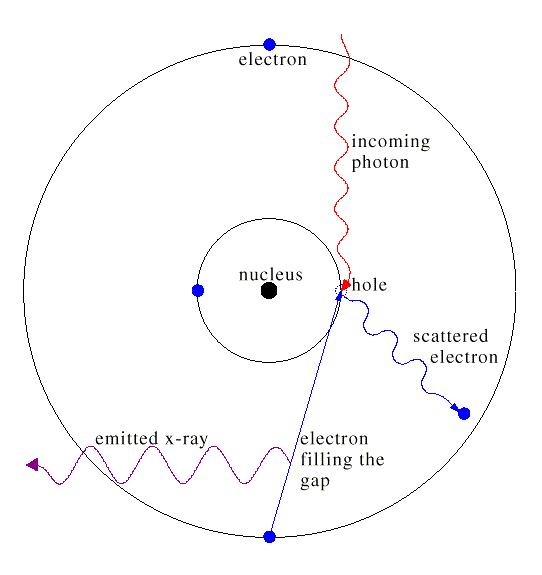
پرتوهای یون ساز کاربردهای پزشکی . کشاورزی و صنعتی داشته در هنگام استفاده از این پرتو ها باید به نکات حفاظتی تماس با آن توجه و رعایت شود از جمله حفاظ گذاری و زمان و فاصله مناسب زمان کار توجه نمود . اشعه ایکس جزء پرتوهای یونساز است
اشعه ماوراء بنفش و اشعه مادون قرمز جزء اشعه های غیر یونساز است .اثرات پرتو ماورائ بنفش شامل قرمزی پوست . تیرگی پوست . سرطان پوست و التهاب قرنیه میباشد . هنگام تماس برای حفاظت در برابر آن باید به نکات حفاظتی از جمله آموزش . فاصله از منبع اشعه . ووسایل حفاظت فرذی و محصور کردن توجه کرد
خورشید یکی از تولید کنندگان این اشعه است
اشعه مادون قرمز از اجسام ملتهب منتشر شده ( جوشکاری ) می تواند باعث آب مروارید شود
گشاورزان . جوشکاران .رادیواوزیستهاو آجرپزها در معرض لشعه هستند
* گرما سرما رطوبت
شرایط جوی محیط کار شامل گرما و سرما و رط.بت می باشد
- گرما و رطوبت
گرمای موجود در محیط کار از منابع مختلفی مثل ماشین آلات . فرایندهای تولید تابش خورشید و وسائل روشنائی وشرایط خارج از محیط کار ایجاد می شود . عوارض آن به دو گروه خفیف وشدید تقسیم می شود .
خفیف شامل سوختگی پوست و جوش گرمائی و شدید شامل گرمازدگی . ضعف گرمائی می باشد . برای کنترل گرمای محیط کار روش های متعددی وجود دارد مانند کاهش فعالیت جسمانی . برنامه منظم کار واستراحت . تهویه عمومی و استفاده از وسائل حفاظت فردی
- سرما
تمروزه مطلوب ترین دما برای زندگی 21 درجه سانتی گراد است . در دمای پائین کار وفعالیت دشوار می شود . اگر سرما شدید باشد دست و پاهای فرد حالت کرخی پیدا کرده و فرد توان انجام کار راندارد . در این حالت استفاده از دستکش ووسائل حفاظت فردی . استفاده از غذا و نوشیدنی ها یگرم . استفاده از پوشاک گرم و برنامه ریزی برای گرم شدن هنگام استراحت می تواند از عوارض سرما جلوگیری نماید
عوارض ناشی از سرما عبارتند از :
- کهیر - سرخی - سرمازدگی
همچنین استفاده از از اتاقک و چادرهای ویزه برای کسانی که در فضای باز کار می کنند پیشنهاد می گردد
کشاورزان .کارگران راه سازی . جنگل بانان و کارگران کوره های آجر پزی در معرض عوارض ناشی از سرما و گرما هستند .
*** فشار هوا و جریان الکتریکی نیز جزء عوامل زیان آور فیزیکی می باشند
2- عوامل زیان آور شیمیائی
عوامل زیان آور شیمیائی محیط کار به سه دسته گردو غبار . دود ودمه . گاز و بخار و کلیه مواد شیمیائی وسموم که در صنعت و کشاورزی استفاده و کارگران در معرض آن هستند تقسیم می شود
کنترل عوامل شیمیائی در بهداشت حرفه ای شامل اقدامات و روش هایی است که برای حذف یا کاهش تماس افراد با عوامل زیان آور محیط کار انجام گرفته یا بکار بسته می شود هدف پایانی همه آنها جلوگیری از اثرا ت سوء عوامل زیان آور برروی کارکنان است . این اقدامات شامل دودسته اقدامات محیطی و فردی می باشد
عوامل کنترلی محیطی شامل
1- طراحی و جانمائی مناسب 2- حذف یاکاهش آلاینده در محل تولید
3- جداسازی 4- تهویه ( عمومی و موضعی )
5- استفاده از روش تر 6- نظافت کارگاه . انبار کردن مواد و برچسب گذاری
عوامل کنترلی فردی شامل :
1- روش انجام کار 2- وسائل حفاظت فردی
3- کاهش زمان کار 4- بهداشت فردی 5- دیگر اقدام ها ( معاینه پزشکی . آموزش بهداشت و ....)
3- عوامل زیان آور ارگونومیکی
این عوامل عبارتند از طراحی نادرست ابزار . تجهیزات و محیط کار نیز حمل و بلند کردن بار . شرائط بینائی نا مطلوب . ارتعاش وضعیت نامطلوب بدنی هنگام کار اعمال نیرو و تکرار حرکت .
هر یک از عوامل یاد شده اگر از اندازه تحمل فیزیواوزیک بدن انسان فزونی گیرد . عوارض و آسیب هایی راایجاد می کند . در بهداشت حرفه ای کوشش ها بر پیش بینی . تشخیص . ارزیابی ودر صورت نیاز کنترل آنها متمرکز است
4- عوامل زیان آور زیست شناختی ( بیولوزیکی )
این عوامل عبارت هستند از حشرات . کپک ها . قارچ ها . باکتری ها . ویروس ها . ریکتزیاها و کلامیدها . این عوامل ممکن است به هنگام کار با نمونه های زیست شناختی . گیاهان . جانوران و یادفع نادرست مواد زاید وفاضلاب . رعایت نکردن بهداشت فردی و نظم و نظافت تولید شوند . در برخی شغل ها به دلیل شرائط کار .گونه فعالیت و نیز تولید یا مصرف مواد گوناگون کارکنان در برابر عوامل زیست شناختی زیانآور ودر نتیجه . ابتلا به بیماریهای عفونی قرار دارند
برنامه ها بهداشت حرفه ای
1- آزمایشات پزشکی قبل از استخدام
2- معاینات دورهای
3- معاینات استخدامی
4- نظارت بر خانه ها بهداشت وبهورزان در روستا در خصوص پیگیری مسائل بهداشت حرفه ای
5- نظارت بر کارخانجات و بازرسی ماهانه
6- طرح بهگر
7- طرح بقاء ( بهداشت قالی بافان ) طرح مشترک جهاد کشاورزی و وزارت بهداشت
8- طرح بهسازی کلرگاههای قالیبافی ( طرح اختصاصی وزارت بهداشت در بهداشتی نمودن کارگاههای قالی بافی )
9- طرح صنوف
10- طرح یایش کارگاههای شهری ( بازدید از کارگاههای سطح شهر )
11- آموزش موازین بهداستی و ایمنی به کارگران . کارکنان . کشاورزان در ارتباط با شغل آنها
12- شناسائی . ارزیابی وکنترل عوامل زیان آور محیط کار
13- اندازه گیری عوامل زیان آور محیط کا ر ( صدا سنجی – نورسنجی – اندازه گیری گاز و بخارات )
14- صدور مجوز ها بهداشتی به کارخانجات
15- بازدید از ترمینال
16- ارجاع به دادگاه
17 - برنامه های مربوط به تغذیه کارگران
18 - توانبخشی حرفه ای
19- بازدید از معادن
دامنه فعالیتهای بهداشت حرفه ای به اختصار عبارتنداز :
1- مسئله بررسی و کنترل بیماریهای ناشی از کار
2- پیشگیری از حوادث ناشی از کار
3- معاینات پزشکی در صنعت
4- تسهیلا ت بهداشتی در صنعت
اساسا بهداشت حرفه ای بیشتر پیشگیری است تا درمان و برای پیشگیری ابتدا با اثر های متقابل محیط کار و خطرهای کاری . علل حوادث و دشواریهلی صنعتی شدن لازم می باشد
-
 مدیر بازنشسته
مدیر بازنشسته

محافظت کننده های پرتوی
کشف محافظهایپرتویبعضی از مواد گرچه بر حساسیت پرتوی سلولها تاثیر مستقیمیندارند اما با ایجاد انقباض عروقی یا مداخله در فرایندهای طبیعی باعث کاهش غلظتاکسیژن در اندامهای بحرانی می شوند . بنابراین کل موجود زنده دربرابر تشعشع محافظتمی شود . به دلیل آنکه سلولها در شرایط هیپوکسی به اشعه ایکس حساسیت کمتری نشان میدهند ، رخداد این فرایند را نیز می توان حفاظت تلقی کرد . مثالهایی از این مواد ،سیانید سدیم ، مونوکسید کربن ، اپی نفرین ، هیستامین و سروتونین می باشد . چنینترکیباتی به خودی خود محافظ پرتوی واقعی به حساب نمی آیند ، لذا بیش از این موردبحث واقع نمی شوند .
قابل توجه ترین گروه محافظهای پرتوی واقعی ، ترکیبات سولفیدریل می باشند . ساده ترین آنها سیستئین است ؛ یک ترکیب سولفیدریل شامل یک اسیدآمینه طبیعی با فرمول زیر است:
NH2
SH – CH2 – CH
COOH
درسال 1984 ، پت دریافت اگر پیش از تابش گیری موشها مقدار زیادی سیستئین به آنهاتزریق یا خورانده شود باعث محافظت موشها از آثار تابش گیری تمام بدن می شود . تقریباً در همان زمان باک و همکارانش در اروپا به طور مستقل قابلیت حفاظت سیستامینرا در برابر تابش گیری تمام بدن حیوانات گزارش کردند . این ترکیب ساختمانی شبیهفرمول زیر دارد :
SH – CH2 - CH2 – NH2
در حیوانات تزریق شدهبا mg/kg 150 سیستامین برای ایجاد مرگ و میز به میزان مشابه با حیوانات کنترل ، به8/1 برابر اشعه ایکس بیشتر نیاز است . این فاکتور 8/1، « فاکتور کاهش دز » DRF نامدارد که به شکل زیر تعریف می شود :
دز تشعشع در غیاب دارو / دز تشعشع در حضوردارو = DRF
مکانیزمعملبرای یافتن محافظهای پرتوی موثر بسیاری از ترکیبات مشابهمورد آزمایش قرار گرفتند . موثرترین آنها از ترکیبات و ویژگیهای معینی برخوردارند : یک گروه آزاد ( یا گروه SH فعال ) در یک طرف مولکول و یک عامل بازی قوی مانند آمینیا گوآنیدین در طرف دیگر قرار می گیرد که با زنجیره مستقیم دو یا سه اتم کربن از همجدا می شوند . ترکیبات سولفیدریل محافظهای پرتوی موثری در مقابل پرتوهای یونسازپراکنده مانند اشعه ایکس یا گاما می باشند . مهمترین مکانیزمهایی که به واسطه وجودگروه SH- در حفاظت سلولی ایجاد می شود ، شامل موارد زیر است :
1- جاروب رادیکالآزاد که در مقابل تولید رادیکال آزاد اکسیژندار با پرتوهای یونساز یا عواملی شیمیدرمانی مانند عوامل آلکیله کننده محافظت به عمل می آورد .
2- اهدای اتم هیدروژنبرای تسهیل ترمیم شیمیایی در نقاط آسیب DAN.
در فصل اول ، درمورد زنجیره وقایعیکه بین جذب فوتون و آسیب بیولوژیکی نهایی روی می دهد ، توضیح داده شد . این مواردشامل تولید رادیکالهای آزاد، پیش از اندرکنش با مولکولهای حیاتی جاروب و حذف شوند ،اثر تشعشع کاهش می یابد . این فرایند در شکل 9-1 نمایش داده شده است .
اثرحفاظتی ترکیبات سولفیدریلی به موازات اثر اکسیژن صورت می گیرد ، بیشترین اثر برایپرتوهای یون ساز پراکنده ( برای مثل اشعه ایکس و گاما ) و کمترین اثر برای پرتوهاییونساز متراکم ( مانند ذرات آلفای کم انرژی ) گزارش شده است . ممکن است پیش بینیشود که بالاترین مقدار ممکن فاکتور کاهش دز با جاروب موثر رادیکالهای آزاد ، معادلنسبت افزایش اکسیژن یعنی مقدار 5/2 تا 3 باشد .
توصیف ساده مکانیزم عمل محافظهایپرتوی سولفیدریل از نظر ظاهری راضی کننده است اما کل داستان نیست ؛ زیرا محافظتهایپرتوی خاصی از این گروه ، در مقابل پرتوهای یونساز متراکم ( مانند نوترون ) بهمیزان بیشتر از حد انتظار موثر خواهند بود . البته عوامل دیگری باید دخالت داشتهباشند که به خوب شناخته نشده اند .
توسعه ترکیبات موثرترجای تعجب نیست کشف ترکیبیکه بتواند در مقابل تشعشع حفاظت ایجاد کند، علاقه و هیجان زیادی را در ارت آمریکاایجاد کرده باشد زیرا در سالهای اول پس از جنگ جهانی دوم هنوز خاطره هیروشیما وناگازاکی در اذهان زنده بود . علی رغم محسوب شدن سیستئین به عنوان یک محافظ پرتوی ،این ترکیب یک ماده سمی است و در دزهایی که حفاظت ایجاد می کند باعث حالتهای تهوع واستفراغ می شود . ارتش ایالات متحده در سال 1959 به منظور بررسی ، سنتز و شناساییداروهای قادر به ایجاد حفاظت پرتوی ، بدون ایجاد سمیت سیستئین و سیستامین برنامهگسترده ای را در موسسه والترررید شروع کرد . در این خصوص بیش از 4000 نوع ترکیبسنتز و آزمایش شد . در مرحله اول کشف مهمی صورت پذیرفت ، مبنی بر اینکه سمیت ترکیبرا می توان تا حد بسیار زیادی با پوشش گروه سولفیدریل با یک گروه فسفات کاهش داد . این مساله در جدول 9-1 نشان داده شده است . دز کشنده 50 درصد ترکیب در حیوانات ، درصورت پوشش گروه SH سیستامین با فسفات تا دو برابر افزایش می یابد و در اثر حفاظتینیز در اصطلاح فاکتور کاهش دز ، تا حد زیادی بهبود حاصل می شود . شایان ذکر است اینعمل موجب کاهش سمیت سیستمیک می شود . با لخت شدن گروه فسفات در سلول ، گروه SH شروعبه جاروب رادیکالهای آزاد می کند .
ساختمان سه ترکیب نمونه از بیش از چهار هزارنوع ترکیبهای سنتز شده سریهای والترید در جدول 9-2 نشان داده شده است . گفته می شوداولین ترکیب ، 683- WR ، سیستافاس نامیده شد . این ترکیب به طور متداول در بستههای سازمانی به وسیله جاسوسان روسی در اروپا طی دوران جنگ سرد برای استفاده درهنگام درگیری های هسته ای حمل می شود . مفید بودن ترکیب مذکور باید تا حد بسیارزیادی از نظر روانی و تقویت روحیه بوده باشد؛ زیرا حمل ترکیب به صورت قرص و تجویزآن خوراکی بود . در واقع ترکیبات سولفیدریل در اسید معده شکسته می شود و تنها زمانیموثر واقع می شوند که به صورت داخل صفاتی یا داخل وریدی تزریق شوند . البته عاملدیگر آن است که چنین ترکیباتی فقط در مقابل پرتوهای یونساز پراکنده حفاظت به عمل میآورند ؛ بنابراین ، حفاظت کمی در مقابل رهایی آنی نوترونهای تولید شده از انفجارهسته ای ایجاد خواهند کرد . این ترکیبات در مقابل پرتوهای گامای ناشی از ریزش اتمینیز موثر می باشند .
دومین ترکیب ، 2721- WR ، امروزه معروف به آمیفوستین ،احتمالاً موثرترین ترکیب سنتز شده در برنامهم والتررید است . حفاظت خوبی را برایاندامهای خونساز ایجاد می کند چنان که مشاهده شد با استفاده از آن فاکتور کاهش دزبرای مرگ 30 روز موش به حداکثر مقدار فرضی سه نزدیک می شود – احتمالاً ترکیبی است که به وسیله فضانوردان امریکایی در سفر به ماه حمل شد تا هنگامرخداد انفجارهای خورشیدی مورد استفاده قرار گیرد . در این ماموریتها ، در صورت خارجشدن سفینه فضایی از مدار زمین و آغاز فرود آمدن آن به سمت ماه ، فضانوردان مجبوربه اجرای ماموریت 14 روزه بودند زیرا سوخت کافی برای چرخش در اطراف ، بدون دور زدندر اطراف ماه و استفاده از میدان جاذبه آن به همراه نداشت . اگر در آن دوره رخدادخورشیدی عمده ای روی می داد ، فضانوردان تحت تابش بارانی از پروتونهای پر انرژیقرار می گرفتند . در این صورت به طور تخمینی بارش مذکور دریافت دزی حدود چندین گری( چند صد راد ) منجر می شد . در چنین موقعیتی در دسترس بودن محافظی پرتوی با فاکتورکاهش بین 2 تا 3 بسیار مهم بود . چنان که دیدیم ، هیچگونه رخداد خورشیدی مهمی طیماموریتهای انسان به ماه روی نداد . از سوی دیگر آمیفوسین از قابلیتهایی درپرتودرمانی نیز برخوردار است که متعاقباً با جزییات بیشتر مورد بحث قرار می گیرد.
سومین ترکیب ، 1607-WR ، ساختمانی شبیه دو مورد دیگر دارد ، اما در واقع به عنوانسم موش صحرایی d-CON به بازار عرضه شده است . این دو دارو با ایجاد توقف قلبی موجبمرگ می شود و در مقایسه با دو عامل دیگر فهرست شده در جدول 9-2 محافظ پرتوی بسیارموثرتری است . داروی مذکور با دز یک صدم حفاظت مشابه ایجاد می کند اما به دلیل سمیتآن مورد مصرف ندارد . این ترکیب در جدول 9-2 نیز گنجانده شده است زیرا نشان می دهدچگونه تغییری کوچک در ساختمان یک ترکیب می تواند به تغییر عمده خصوصیت و ویژگی منجرشود ؛ از سوی دیگر از منظر سمیت سلولی محدود کننده دز در سری ترکیبات سولفیدریل نیزقابل توجه است ؛ سمیت محدود کننده دز آمیفوستین کاهش فشار خون می باشد
-
 مدیر بازنشسته
مدیر بازنشسته

دید کلی
مشکل مربوط به راکتورهای شکافتی آن است که از انرژی آنها برق تولید میشود. مقدار زیادی انرژی به صورت زبالههای رادیواکتیو باقی میماند. در استفاده مجددا از عناصر سوختی ، مقداری زیاد و خطرناک از انواع عناصر رادیواکتیو باقی میماند. وجود زبالههای واجد تابش بسیار ، یکی از خطرات همیشگی برای زندگی بشر امروزی به شمار میآید. میتوان در ظرف فولادی ضدزنگ این زبالهها را به مایع تبدیل کرد. اما چون اتمهای انرژیدار آنها گرما ایجاد میکنند، از این رو یک سیستم خنک کننده دائمی ضرورت پیدا میکند. گازهایی نیز تولید میشوند که در صورت نشت خطرناک هستند.
روشهای دفع زبالههای هستهای
میتوان زبالهها را در تابوتهایی در اعماق اقیانوسها دفن کرد. اما این خطر وجود دارد که بر اثر فعالیتهای شدید دریایی از آنجا فرار کرده یا شکسته شوند.
میتوان زبالههای هستهای را توسط موشک در درون فضا پخش کرد. اما این عمل هم با اعتراضاتی مواجه شد، و نیز شبهههایی وجود دارد که در صورت شکست پرتاب موشکها ، امکان آلودگی کره زمین وجود دارد. 
استفاده از نشت هیدرولیکی روش دیگر میباشد. یعنی حفرههایی در سنگها ایجاد کرد. و با استفاده از فشار هیدرولیکی سنگ رسی را به صورت افقی قطع میکنند. سپس زبالههای رادیواکتیو مانند لایهای در داخل ساندویچی در داخل مایع سیمانی پخش میشوند.
یکی دیگر از پیشنهادهای محتمل ، استفاده از معدن نمک است. دفع نهایی به هر طریق که صورت گیرد، روش آماده سازی برتر زبالهها این است که آنها را در سرامیکهایی که عناصر رادیواکتیو از آنها قابل نشت هستند، به صورت متبلور در آورند.
مقایسه زبالههای هستهای با مواد انفجار ی بزرگ
نکته جالب در این است که بشر با زبالههای هستهای حاصل از شکافت هستهای ، به گونهای برخورد میکند که با فرآورده های حاصل از مهبانگ رفتار شد. در حدود 4.5 میلیارد سال قبل ، در یک بازوی مارپیچ نزدیک به لبه کهکشان راه شیری ، تشکیل منظومه شمسی ما آغاز شد. ستاره مورد نظر خورشید ، تشکیل گردید و در اطراف آن گلوله برفیهای مواد شکل گرفته ، با یکدیگر برخورد نمودند و در هم تلفیق شدند، تا اینکه برخی از آنها سیاره زمین را درست کردند. تعدادی از آن مواد زباله هستهای رادیواکتیو مهبانگ بود که در سنگهای ستاره ما قرار داده شد. انسان معدن قابل شکافت را از آن سنگها استخراج کرده و مورد استفاده قرار داد. در حال حاضر انسان نمیداند چگونه آنها را به زمین باز گرداند.
-
 مدیر بازنشسته
مدیر بازنشسته

آثار وراثتی تشعشع در انسان
کمترین دز مضاعف کننده ممکن برای انسان Sv 03/0 ( rem 3 ) می باشد زیرا این مقدار ، مقدار متوسط تشعشع دریافت شده از منابع طی دوران 30 ساله باروری است . چنین مقداری برای دز مضاعف کننده ، به معنای ناشی شدن تمام جهشهای خودبخود از تشعشع زمینه است ، که البته بسیار ناممکن می باشد. بازماندگان حمله بمبهای اتمی در هیروشیما و ناگازاکی ، بزرگترین جمعیت انسانی تابش دیده را تشکیل می دهد و بدقت برای بررسی آثار وراثتی مورد مطالعه قرار گرفته است . طی سالها ، گروهی از 3115 فرزند والدینی که مقادیر قابل توجهی از تشعشع را دریافت کرده بودند ( یعنی در Km 2 نزدیک مرکز انفجار بمب ) و گروه کنترل تا حد بیشتر 41066 با توجه به شاخصهای گوناگون مورد مطالعه قرار گرفتند : در سالهای اول بعد از تولد برای نقصان مادرزادی ، جنسیت کودک ، توسعه و رشد فیزیکی و بقا ( زنده ماندن ) ، سپس در میانسالی برای ناهنجاری های سیتوژنتیکی و اخیراً برای بیماریهای بدخیم و نقصهای عملکردی و الکتروفورتیک چیزی حدود 30 نوع پروتئین سرم یا آنزیمها و اریتروسیتها بررسی شده است . هیچ یک از شاخصها به طور قابل توجهی به تابش گیری والدین ربط داده نشد ، اما رگرسیون خالص تا حد کمی مثبت بود 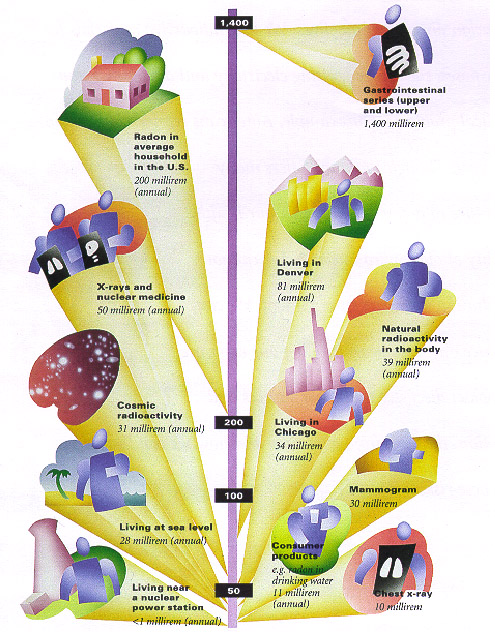
برای بررسی موارد گوناگون آثار وراثتی ، تفاوتهای بین کودکان بازماندگان تابش دیده مربوط به فواصل نزدیک یا دور از محل انفجار مورد نظر است ، اما در واقع هیچ یک از یافته ها از نظر آماری معنی دار نیست . به هر حال برای محاسبه دزهای مضاعف کننده از تفاوتهای بین این گروههای کودکان استفاده شده است . این بحث وجود دارد که حتی در صورت عدم وجود تفاوت معنی دار آماری ، استفاده از این اطلاعات برای تخمین دزهای مضاعف کننده مجاز است . دلیل این مسأله مورد تردید بودن رابطه بین تابش گیری از تشعشع و ناهنجاری های مادرزادی می باشد زیرا یافته های جانوری ،بودن چون و چرای آن را تبیین کرده است . البته علاوه بر آن آسیبهای کروموزومی مشاهده شده در بازماندگان نیز مؤید این وضعیت می باشد .
تنها سه مورد از این شاخصها برای تخمین دز مضاعف کننده ، مورد استفاده دارد . در این خصوص نتایج برگرفته از مطالعه ای در اوایل دهه 1980 در جدول 11-2 نشان داده شده است . میانگین ساده این سه تخمین Sv 56/1 (rem 156 ) می باشد . در یک مقاله مروری جدیدتر ، نیل دز مضاعف کننده برای انسان را حدود Sv 2 _ که البته بسیار تردیدانگیز می باشد _ تخمین زد ، حد پائینی تخمین Sv1 و یک حد بالایی متوسط پیش بینی شده است . البته این تخمین به دز تشعشعی حاد مربوط می شود زیرا به بازماندگان ژاپنی بستگی دارد .
این تخمین برای انسان باید با رقم قابل مقایسه ای حدود Gy 39/0 ( rad 39 ) برای دزهای مضاعف کننده در موش در خصوص تابش گیری حاد از تشعشع با انتقال انرژی خطی کم مقایسه شود ( پیش از این رقم Gy 1 برای دز مضاعف کننده ذکر شده برای آهنگ دز کم بود ) . اطلاعات پراکنده انسان مورد اخیر را _ که دزهای مضاعف کننده ، حاصل از آزمایشهای با مکان ژنی خاص موش ، بسیار پائین می باشند _ تایید می نماید .
اصول تعیین مخاطره وراثتی در انسان ممکن است به صورت زیر جمع بندی شود:
1- بیشتر جهشها ، خواه خودبخود یا القا شده با تشعشع مضر می باشند ؛
2- هر دزی از تشعشع ، هر چند کم ، مخاطره هایی از اثر وراثتی را در بر دارد اما تشعشع یک جهش زای نسبتاً ضعیف است ؛
3- تعداد جهشهای تولید شده متناسب با دز است به گونه ای که یک تعمیم خطی از اطلاعات حاصل از دز بالا ، تخمین معتبری را برای آثار مربوط به دز کم فراهم می آورد ؛
4- تخمینهای مخاطره بر مبنای آزمایشهای انجام شده با موش است .
شرایطی که در آن انسان _ خواه به عنوان عضوی از جامعه ، خواه در دوره اشتغال _ تحت تابش اشعه قرار می گیرد ، باعث ایجاد میزان جهشهایی به میزان کم می شوند ؛ به عبارت دیگر یا آهنگ دز در شرایط تابش گیری پیوسته بسیار کم است یا اگر آهنگ دز بالا است ، میزان دز به ازای هر جلسه تابش کم می باشد . در هر یک از موارد ، اطلاعات حاصل از موش نشان دهنده رخداد جهشهای کمی است . در موارد نادر که دزی زیاد در یک تابش گیری حاد جذب می شود ، برای مثال ، در یک سانحه تشعشعی ، بخش عمده ای از عواقب وراثتی کشنده را می توان با تأخیر در آمیزش حذف کرد . در این خصوص برای یک مرد ، دوماه کافی است ؛ دوره قابل مقایسه برای زنان به طور قطع مشخص نیست ؛ اما احتمالاً طولانیتر از مردان است . با توجه به پیشنهاد قبلی، یک روش محافظه کارانه ، توصیه به مردان و زنان در خصوص پرهیز از آمیزش حداقل به مدت 6 ماه پس از تابش گیری از تشعشع قابل توجه ، برای کاستن از خطر ناهنجاریهای وراثتی است .
__________________
-
 مدیر بازنشسته
مدیر بازنشسته
-
 مدیر بازنشسته
مدیر بازنشسته
-
 مدیر بازنشسته
مدیر بازنشسته
-
 مدیر بازنشسته
مدیر بازنشسته
-
 مدیر بازنشسته
مدیر بازنشسته

خطرات پرتو ايکس را مهارکنيم
بشر از دير باز ارتباطي ويژه با نور داشته است و همواره سعي داشته از اين نعمت پروردگار بيشتر در زندگي خود استفاده نمايد و با گذشت زمان دريافت، اين نيروي خارق العاده قابليتهايي فراوان دارد و كمر به كشف آنها بست و امروزه سعي كرده از اين آفريده ايزد منان به عنوان فنآوري برتر در بخشهاي مختلف علمي، صنعتي، ارتباطي، پزشكي و... استفاده نمايد. به طور مثال در زمينه پزشكي از اشعه ايكس كه سرمنشايي از نور دارد جهت تشخيص و
بشر از دير باز ارتباطي ويژه با نور داشته است و همواره سعي داشته از اين نعمت پروردگار بيشتر در زندگي خود استفاده نمايد و با گذشت زمان دريافت، اين نيروي خارق العاده قابليتهايي فراوان دارد و كمر به كشف آنها بست و امروزه سعي كرده از اين آفريده ايزد منان به عنوان فنآوري برتر در بخشهاي مختلف علمي، صنعتي، ارتباطي، پزشكي و... استفاده نمايد. به طور مثال در زمينه پزشكي از اشعه ايكس كه سرمنشايي از نور دارد جهت تشخيص و درمان بيماران استفاده ميگردد.
همانطور كه ميدانيم تابش بهصورت انرژي و يا ماده حامل انرژي است و اگر ماده اي كه تحت واكنش قرار ميگيرد، ارگانيسم زنده باشد، اثرات به هم كنش ميتواند تا مرحله بيماري شديد و يا مرگ به بافت زنده آسيب برساند. مردم تا حدي بهطور تصادفي به طبيعت زيان بخش تابش بر روي بافت زنده آگاهي يافتند. ابتدا سوختگيهاي بر روي پوست كارگراني كه تحت تابش قرار ميگرفتند مشاهده شد و متاسفانه قبل از اينكه صدمات ناشي از تابش شناخته شود، مواردي از مرگ و جراحات شديد در اثر پرتو گيري اتفاق افتاد.
در سالهاي 1299/1920 (25 سال پس از كشف پرتوهاي X) بود كه معيارهاي ايمني براي كار با مواد پرتوزا پيشنهاد شد. و در سالهاي 1309/1930 قوانيني جهت اطلاع از مقدار ماكزيمم سطوح مجاز پرتوگيري وضع شد به مقدار تابش معمولا به عنوان "دوز" اشاره ميشود. نكته حايز اهميت تشخيص تفاوت بين پرتوگيري و دز دريافتي است. براي حفاظت شخصي، پرتوگيري مورد توجه قرار ميگيرد، در حاليكه براي صدمات زيست شناختي (يا ساختماني) دز جذب شده حائز اهميت است.
دوز فيزيكي جذب شده پرتوها- kvx 250براي ايجاد يك اثر معين
دو.ز فيزيكي جذب شده توسط تابش مقايسه اي براي ايجاد اثر مشابه
حداكثر پرتوگيري مجاز براي هر فرد را ميتوان بدون توجه به نوع تابش بر حسب rem بيان كرد.
دز بر حسب راد×rem = QF
پرتو گيري تابش به دو طريق صورت ميگيرد : 1 - پرتوگيري خارج بدن يا البسه به طور مستقيم از يك چشمه.
2 - پرتوگيري داخلي چشمه هايي كه از طريق استنشاق، فرو بردن و يا جذب وارد بدن شده اند.
پرتودهي يك سلول ممكن است باعث صدمة هسته سلول يا اجزاي ديگر آن شود. در اين صورت ممكن است كه سلول از بين برود و يا كروموزمهاي سلولي كه در حال توليد مثل هستند تغيير يابد و باعث تحول در سلول شود و اين بدان معناست كه فرزندان كم و بيش معيوب خواهند بود و اين عيوب ممكن است به نسلهاي بعد منتقل شود. راهنماي حفاظت در مقابل تابش NCRP (راهنماي تابش براي پرتو گيري مجاز افرادي كه در نواحي تابش كار ميكنند ) براي افرادي كه بواسطه شغل خود در معرض تابش قرار ميگيرند، به قرار زير است :
1- كل دوز دريافتي تمام بدن در طي سالها بايد حداكثر برابر (18- n)5 rem باشد كه در آن n =عمر شخص است بايد توجه كرد كه افراد كمتر از 18 سال مجاز نيستند در محلي كه در معرض تابش قرار دارد، كار كنند،
2 - دوز دريافتي نبايد از 5 rem در سال تجاوز نمايد و
3 - همچنين ماكزيمم پرتوگيري بجز براي پوست، دستها و ساعد نبايد در مدت 13 هفته از 5 rem بيشتر باشد.
قسمتهاي خاصي از بدن ميتوانند تابش بيشتري دريافت دارند، ولي راهنما معمولاً براي تمام بدن در نظر گرفته شده است. در حال حاضر مسئله اساسي ايجاد حفاظت در مقابل "1- اشعه گاماي اوليه 2 - تابش ايجاد شده در نتيجه واكنشهاي r - n در حفاظ. 3- نوترونهاي سريع" است حفاظ در ساده ترين شكل، متضمن ايجاد فاصله و قرار دادن مواد بين اشعه و گيرنده تابش است.
اگر فاصله كافي بين شخص و چشمه وجود داشته باشد، شدت تابش به سطوح ايمن كاهش مييابد. با وجود اين اگر ماده اي بين ما و چشمه قرار بگيرد ميتوان از امتياز تضعيف ايجاد شده توسط ماده استفاده كرد.
با توجه به مطالب ذكر شده لزوم استفاده از تجهيزات حفاظتي در برابر تاثيرات مضر پرتوهاي يونيزان روز به روز در حال افزايش است. در اين راستا آژانس بين المللي انرژي اتمي IAEA با تدوين آيين نامه ها و راهكارهاي اساسي در جهت استفاده درست و بي خطر از دستگاها و تجهيزات و منابع توليد كننده پرتوهاي يونيزان و خطرناك كمك شاياني را در پيشگيري از اثرات پرتوها به عمل آورده است.
همانطور كه گفته شد جهت مهار كردن اشعه اي كه در فضا انعكاس پيدا ميكند، بايد سرعت آنرا با استفاده از عناصري كه داراي عدد جرمي بالايي است به حد اقل برساند مانند عناصر طلا يا سرب كه البته با توجه به مقرون به صرفه بودن بيشتر از سرب استفاده ميشود و به همين جهت در بخشهايي از مراكز درماني مانند بخشهاي راديولوژي، آنژيوگرافي و اتاق عمل كه مستقيماً با اشعه سرو كار دارند براي حفظ امنيت اطرافيان در ديوارها و دربها در اطراف دستگاه از سرب استفاده ميشود. اما پزشكان يا تكنسيني كه در داخل اتاق اشعه به سر ميبرند چه بايد بكنند ؟ مشخصاً عوامل حفاظتي ويژه اي براي اين افراد طراحي گرديده است. مثلا از پاراوانهاي سربي و همچنين روپوشها و شيلدهاي سربي جهت حفاظت در برابر اشعه استفاده ميشود. در اين راستا شركت نويد پرتو نما با داشتن سالها تجربه و كادري مجرب و متخصص در زمينه توليد، واردات و صادرات تجهيزات و لوازم راديولوژي و پوششهاي محافظ اشعه X افتخار دارد تا خود را به عنوان يكي از شركتهاي مطرح در اين عرصه به شما متخصصان، پزشكان و كارشناسان محترم كه در تماس با پرتوهاي يونيزان خطرناك ميباشيد معرفي كند.
شيشه سربي
يكي ديگر از مواردي كه لزوم استفاده آن در بخشهايي شامل دستگاه پرتوزا ضروري مينمايد شيشه سربي است. در اينجا جهت آشنايي شما خوانندگان محترم با اين محصول خلاصه اي از ساخت آنرا تشريح مينمائيم.
ابتدا سرب را در كورههاي صنعتي به صورت مذاب درآورده، سپس آنرا درون مخازن پيستوله مانندي ريخته و با توجه به قطر و سايز مورد نظر ميزان فشار و روزنه خروج عنصر را تنظيم ميكنند تا آنرا به صورت غبار و گرده خارج كنند. به حجم غبار سرب نيز "مش" گفته ميشود به طور مثال براي توليد سرب 1/0 با مش 400، ميزان فشار را تنظيم كرده سپس سرب را درون حوضچههاي آب سرد اسپري ميكند و تمام اين گرده ها با همان اندازه و حجم سرد شده و به صورت خاك سرب در ته حوضچه جمع ميگردد. بعد از جمعآوري خاك سرب، سيليس را در مخازن ديگر ذوب كرده آن را به داخل قالبهاي مورد نظر با قطر و اندازه مشخص هدايت ميكند و دوباره گردههاي سرب را كه با اكسيد سرب بيرنگ شده به گونهاي در فضا پخش ميكنند كه بهصورت يكنواخت و ميزان مورد نظر در ميان سيليس ذوب شده قرار گيرد، بدين ترتيب پس از سرد شدن سيليس، شيشهاي سربي با شفافيت بسيار بالا خواهيم داشت. البته اين پروسه توليد در عين سادگي بيان بسيار پيچيده است و ميبايست دقت عمل زيادي را در توليد آن بهكار گرفت. از معروفترين كمپانيهايي كه اين كالا را با كيفيتي بي نظير در جهان توليد ميكند كمپاني SCHOTT آلمان را ميتوان نام برد. لازم به ذكر است اين كمپاني آلماني داراي استانداردهاي معتبر و قابل اطمينان زيادي از جمله CE،TUV و... است.بيمارستانها و مراكز تخصصي زيادي در حال حاضر در ايران از اين شيشههاي سربي در بخشهاي خود استفاده ميكنند و تا كنون هيچ شواهدي مبني بر عدم كيفيت اين شيشهها گزارش نشده است. استفاده از اين شيشههاي سربي در بخش ها باعث ميشود كه علاوه بر توانايي عبور نور، جلوي عبور اشعه ايكس را بگيرد.
شركت نويد پرتونما با داشتن سالها سابقه در واردات اين نوع شيشه سربي نماينده انحصاري كمپاني SCHOTT آلمان است. ميزان سرب استاندارد جهت شيشههاي سربي كه مورد تائيد سازمان انرژي اتمي ايران ميباشد 2 ميليمتر است كه شيشههاي سربي وارد شده از كمپاني SCHOTT آلمان توسط شركت نويد پرتو نما داراي 1/2 ميليمتر سرب است.
روپوش و اپرون
روپوشها و اپرونهاي سربي از ديگر پوششهاي حفاظتي در برابر اشعه است كه توسط كاربران و يا بيماران مورد استفاده قرار ميگيرد. روپوشهاي سربي مكانيزم ساختاري شبيه به شيشه سربي دارد اما با توجه به اين مسئله كه روپوش را خود شخص بايد استفاده كند و گاه تا ساعتها بايد آنرا به تن داشته باشد. ميزان وزن و انعطاف پذيري آن بسيار مهم است. و علاوه بر آن چون اين نوع شيلدهاي سربي جهت محافظت در برابر اشعه متفرق شده استفاده ميشود. استاندارد ميزان سرب تعريف شده از طرف سازمان انرژي اتمي ايران 5/0 ميليمتر است. ميزان سربي كه در لاستيك قرار ميگيرد بستگي به اكيوالان لاستيك دارد يعني هر چه كيفيت حجم لاستيك بالاتر باشد ميزان جرم بيشتري را قبول ميكند. به طور مثال هنگامي كه لاستيك مذاب جهت نورد شدن به داخل دستگاه ريخته ميشود و از بين غلطكها عبور ميكند چنانچه اكيوالان قطر لاستيك 1 ميلي متر باشد فاصله غلطكها به آن ميزان تنظيم ميشود و به همان ميزان به آن خاك سرب اضافه ميشود. بالاترين مكانيزمي كه در ايران به آن دست يافتهاند 13/0 اكيوالان براي 75/0 ميلي متر است.در صورتي كه اين مكانيزم در خارج از كشور 5/0 اكيوالان براي 1 ميلي متر سرب است. سپس با توجه به اين ضخامت ميتوان از قطر كمتري از لاستيك استفاده كرد در نتيجه وزن روپوش توليد شده كمتر و انعطاف آن بيشتر خواهد شد.
البته امروزه در كشورهاي اروپايي از لاستيكهايي با ساختاري سبك و كيفيت بالا بيشتر استفاده ميشود كه قيمت بالايي دارد اما شخص استفاده كننده بسيار با آن راحت بوده و ميتواند به راحتي با آن كار نمايد.
از جمله اين كمپانيهاي اروپايي Dr.Goos وCAWO و MAVIG از كشور آلمان و Am r ay از كشور ايرلند است. كه نوعي لاستيك سربي بسيار سبك با نام Supra Light استفاده مينمايند.
شركت نويد پرتونما نماينده انحصاري كليه كمپانيهاي فوق بوده و سالها است كه با واردات روپوش و جليقه و دامن سربي از اين كمپانيها جديدترين و مرغوب ترين نوع شيلد سربي را در اختيار كاربران قرار ميدهد.
نسل جديد روپوشهاي محافظ در برابر اشعه X روپوشهاي بدون سرب است كه از يك لايه لاستيك حاوي آلومينيم، صفحه اي كه با مغناطيس باردار شده و پلي اتيلن ساخته شده است. در اين شيلدها ابتدا لاستيك حاوي آلومينيم اشعه را جذب و از طريق لايه مغناطيسي، اشعه منحرف ميگردد و توسط محيط جذب ميگردد كه به علت داشتن چنين ساختماني بسيار سبك و قابل انعطاف است.شركت نويد پرتونما با واردات اين محصول كاملاً جديد (روپوشهاي Lead Free) به ايران از كمپانيهاي آلماني Dr.Goos و MAVIG سعي نموده است در جهت راحتي هر چه بيشتر كاربران قدمي مثبت بردارد.
عينک
عينكها از جمله پوششهاي ديگري است كه درتمام بخشهايي كه در دستگاههاي توليد كننده اشعه ايكس در آن قرار دارد بايد توسط كاربران استفاده شود.
نسل ديگري از اين محصول عينكهايي است كه در قاب كنار عينك نيز سرب بهكار رفته است و معمولاً در آنژيوگرافي و اتاق عمل استفاده ميشود. شركت نويد نماينده انحصاري چند شركت آلماني از جمله CAWO و همينطور چند كمپاني آمريكايي جهت عينكهاي سربي از اين نمونه است.
توليد در ايران
دامنه فعاليتهاي شركت نويد تنها به همين موضوع محدود نميشود اين شركت با داشتن كادري مجرب و دوره ديده از سازمان انرژي اتمي ايران جهت سربكوبي با خالص ترين نوع سرب كه در كشور ما مرغوب ترين سرب، سرب زنجان است، اقدام نموده است.
شركت نويد همينطور با توليدات متنوع و با كيفيت بسيار بالا در انواع روپوشهاي سربي و كليه شيلدهاي محافظ و همينطور تجهيزات مورد نياز تاريكخانه در بخشهاي راديولوژي (ميز تاريكخانه، چراغ اخطار، چراغ تاريكخانه و انواع پاراوانهاي سربي، پاس كاست، كاست استند و...) تنها صادركننده موفق اين اقلام نيز است. در حال حاضر توليدات اين شركت با داشتن معتبر ترين استانداردهاي روز، از مراكز مختلفي مانند سازمان انرژي اتمي ايران، اداره تجهيزات پزشكي،وزارت بهداشت و درمان و آموزش پزشكي و... به شكل وسيعي توسط مراكز تصويربرداري و بيمارستانها و مطبهاي راديولوژي مورد استقبال قرار گرفته است.
در پايان سپاس بر پروردگار كه قدرت و همت پيمودن اين راه سخت و طولاني را در اين مدت به ما ارزاني داشت تا بتوانيم مجموعه حاضر را تقديم متخصصان و كارشناسان محترم رشته راديولوژي و كليه كاربران و مصرفكنندگان اين محصولات بنماييم.
منبع:سایت مهندسی پزشکی وتجهیزات آزمایشگاهی
کلمات کلیدی این موضوع
 مجوز های ارسال و ویرایش
مجوز های ارسال و ویرایش
- شما نمیتوانید موضوع جدیدی ارسال کنید
- شما امکان ارسال پاسخ را ندارید
- شما نمیتوانید فایل پیوست کنید.
- شما نمیتوانید پست های خود را ویرایش کنید
-
مشاهده قوانین
انجمن






 پاسخ با نقل قول
پاسخ با نقل قول

 زباله هسته ای
زباله هسته ای